これまでの電池用電解液は、酸素(O)や窒素(N)をベースとした溶媒が主流でしたが、これらはリチウムイオン(Li+)との結合が強すぎ、電極界面での電荷移動を妨げるという課題がありました。
本研究では、新たに合成したモノフッ素化構造を持つアルカンを溶媒に採用。特に1,3-ジフルオロプロパン(DFP)をベースとした電解液は、これまでの電池の限界を大きく広げる特性を示しました。
開発のポイント
- 脱「酸素・窒素」のリガンド設計: 弱い「F–Li+(フッ素–リチウム)」配位を利用することで、イオンの脱溶媒化をスムーズにし、界面での反応速度を劇的に向上させました。
- 高濃度溶解の実現: 立体障害とルイス塩基性を緻密に設計することで、フッ素ベースでありながら 2 mol l-1 を超える塩の溶解に成功しました。
技術的な詳細と驚異的な性能
1. 極低温下での圧倒的な導電性と反応性
従来の電解液が凍結・高粘度化するような極低温下でも、DFPベースの電解液は高い流動性とイオン伝導性を維持します。
- イオン伝導率: -70度で 0.29 mS cm-1 を達成。
- 反応速度(交換電流密度): -50度において、従来の酸素ベース溶媒よりも1桁(約10倍)大きい値を記録しました。
2. 高いエネルギー密度と実用性
リチウム金属電池において、非常に少ない電解液量(貧電解液条件:0.5 g Ah-1 未満)での動作を可能にしました。
- 重量エネルギー密度(室温): 700 Wh kg-1 超(現在の一般的なリチウムイオン電池の2〜3倍)。
- 重量エネルギー密度(-50度): 約 400 Wh kg-1。
- クーロン効率(CE): 最大 99.7% を達成。
3. 高電圧安定性
- 酸化安定性: 4.9 V を超える高電圧に耐え、高エネルギー密度の正極材料との組み合わせが可能です。
- 低粘度: 0.95 cp と非常にさらさらしており、高速なイオン輸送に寄与しています。
補足:ハイドロフルオロカーボン(HFC)電解質の意義
この研究は、錯体化学の視点から電池のボトルネックを解消した点に大きな意義があります。
- インターフェースの革新: 酸素ベースの溶媒はLiイオンを強く掴みすぎるため、電極に入る際に大きなエネルギーが必要でした。フッ素ベースにすることで、イオンを「ほどきやすく」し、冬場の低温環境や超急速充電での性能低下を防ぎます。
- 次世代航空・宇宙・極地への応用: -50度以下で 400 Wh kg-1 というエネルギー密度を維持できるため、成層圏を飛ぶ航空機や宇宙探査、寒冷地でのEV利用に革命をもたらす可能性があります。
まとめ表
| 項目 | 詳細 |
| 主要溶媒 | 1,3-ジフルオロプロパン (DFP) 等の HFC |
| 配位子タイプ | フッ素 (F) ベースのリガンド |
| イオン伝導率 (-70度) | 0.29 mS cm-1 |
| 酸化安定電位 | 4.9 V 超 |
| エネルギー密度 (室温) | 700 Wh kg-1 超 (ポーチセル) |
| エネルギー密度 (-50度) | 約 400 Wh kg-1 |
| 特徴 | 超低粘度 (0.95 cp)、弱いLi+配位による高速電荷移動 |
このHFC電解質は、従来の液体電解質の延長線上ではなく、全く新しい化学的アプローチによって電池の動作限界を押し広げました。
出典:https://www.nature.com/articles/s41586-026-10210-6
Breakthrough in Next-Generation Batteries: Practicality of Fluorinated Solvents Balancing Ultra-Low Viscosity and High Stability
For decades, electrolyte solvents for batteries have been dominated by oxygen (O)-based and nitrogen (N)-based ligands. However, these solvents bind too strongly with lithium ions (Li+), which creates a bottleneck by hindering the charge transfer process at the electrode interface.
In this research, alkanes with newly synthesized monofluorinated structures were adopted as solvents. Specifically, electrolytes based on 1,3-difluoropropane (DFP) have demonstrated properties that significantly push beyond the current limits of battery technology.
Key Development Points
- Ligand Design Moving Beyond Oxygen and Nitrogen: By utilizing weak “F–Li+” (fluorine–lithium) coordination, the researchers made ion de-solvation smoother, dramatically improving reaction kinetics at the interface.
- Achieving High-Concentration Solubility: Through precise engineering of steric hindrance and Lewis basicity, the team successfully dissolved salts at concentrations exceeding 2 mol l-1, a feat previously difficult for fluorine-based solvents.
Technical Details and Extraordinary Performance
1. Overwhelming Conductivity and Reactivity at Cryogenic Temperatures
Even at ultra-low temperatures where conventional electrolytes freeze or become highly viscous, DFP-based electrolytes maintain high fluidity and ionic conductivity.
- Ionic Conductivity: Achieved 0.29 mS cm-1 at -70°C.
- Reaction Kinetics (Exchange Current Density): At -50°C, the recorded values were one order of magnitude (approx. 10 times) higher than those of conventional oxygen-based solvents.
2. High Energy Density and Practicality
The electrolyte enables the operation of lithium metal batteries under “lean electrolyte” conditions (less than 0.5 g Ah-1).
- Gravimetric Energy Density (Room Temp): Over 700 Wh kg-1 (2–3 times higher than current standard lithium-ion batteries).
- Gravimetric Energy Density (-50°C): Approximately 400 Wh kg-1.
- Coulombic Efficiency (CE): Achieved a maximum of 99.7%.
3. High-Voltage Stability
- Oxidative Stability: Withstands high voltages exceeding 4.9 V, allowing for combinations with high-energy-density cathode materials.
- Low Viscosity: At 0.95 cp, the electrolyte is extremely fluid, contributing to rapid ion transport.
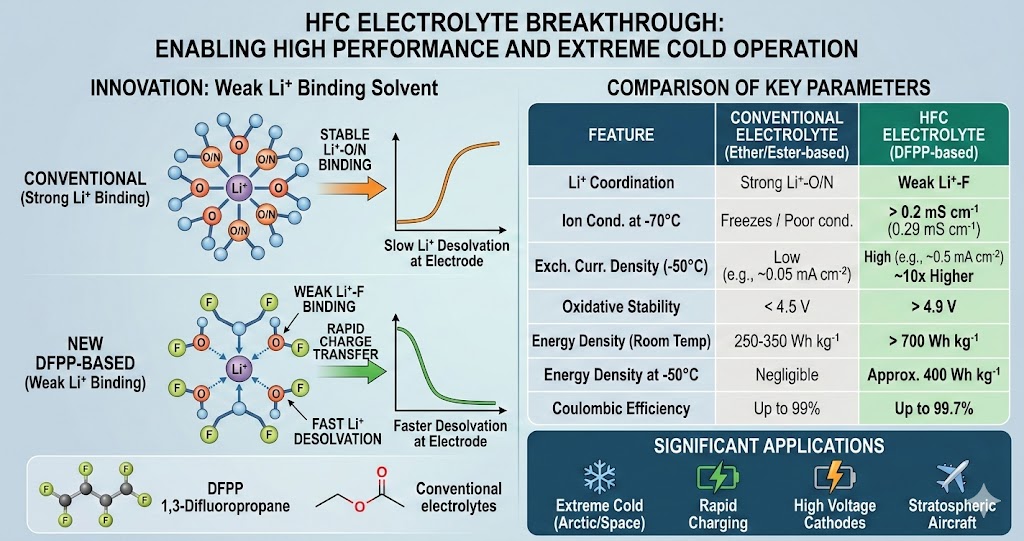
[Image comparing energy density and temperature range of HFC electrolyte vs conventional electrolytes]
Significance of Hydrofluorocarbon (HFC) Electrolytes
This research is significant because it resolves battery bottlenecks from the perspective of coordination chemistry.
- Interface Innovation: Because oxygen-based solvents “grip” Li ions too tightly, a large amount of energy was required for the ions to enter the electrode. Switching to a fluorine base makes it easier for ions to “disentangle,” preventing performance drops in winter environments or during ultra-fast charging.
- Applications for Aerospace and Polar Regions: The ability to maintain an energy density of 400 Wh kg-1 at temperatures below -50°C could revolutionize stratospheric aircraft, space exploration, and the use of EVs in extremely cold climates.
Summary Table
| Item | Details |
| Primary Solvents | HFCs such as 1,3-difluoropropane (DFP) |
| Ligand Type | Fluorine (F)-based ligands |
| Ionic Conductivity (-70°C) | 0.29 mS cm-1 |
| Oxidative Stability Potential | Over 4.9 V |
| Energy Density (Room Temp) | Over 700 Wh kg-1 (Pouch cell) |
| Energy Density (-50°C) | Approx. 400 Wh kg-1 |
| Key Characteristics | Ultra-low viscosity (0.95 cp), fast charge transfer due to weak Li+ coordination |
This HFC electrolyte is not merely an extension of existing liquid electrolytes; it pushes the operational limits of batteries through a completely new chemical approach.


コメント